铝阳极氧化碱蚀槽中游离碱浓度和铝含量的测定
罗一帆,许旋
(1.中山大学北校区化学教研室,广东广州 510089;2.华南师范大学化学系,广东广州 510631)
摘要:根据铝合金碱蚀反应机理,提出了采用单指示剂法、双指示剂法以及EDTA络合滴定法这三种方法来测定铝阳极氧化碱蚀槽液中游离碱和铝的含量。介绍了上述三种测定方法的测定原理,并对它们测定结果的准确性、精密度及操作步骤与成本进行了综合分析与比较。结果表明,上述三种测定方法的精密度与准确性均能满足铝合金氧化加工生产上的要求,但从操作步骤与成本来考虑,单指示剂法最好,双指示剂法次之。
1 前言
碱蚀是铝阳极氧化预处理中的重要工序,是镀层获得均匀色调和表面光泽的主要原因。碱蚀是铝材表面处理的关键步骤,其目的有三个:一是去除铝材表面的自然氧化膜,活化表面,以利于阳极氧化;二是除去表面挤压粗纹等缺陷,使其平整光滑;三是除油净化表面。碱蚀液的主要成分是烧碱及多种有机络合添加剂。随着碱蚀的进行,铝溶解量会逐渐增加,而当其增加到一定程度时,将严重影响碱蚀效果和后续工序的表面处理质量。因此,准确及时地对碱蚀槽液中的游离碱和溶解铝量进行测定,由此可对碱蚀槽液中的游离碱和铝离子含量进行调节,这对提高铝材氧化质量起到非常关键的作用。
本文根据铝材氧化加工过程中铝在碱蚀槽液中的化学作用,分别采用单指示剂中和滴定法、双指示剂中和滴定法和络合滴定法测定碱蚀槽液中游离碱的浓度和溶解铝的含量。三种测定方法虽然都各有优缺点,但均操作简单、方便、准确,都能满足生产的要求。所以在测定碱蚀槽液中的游离碱和溶解铝量时,可选择其中的任何一种方法进行测定。
2 实验原理与实验内容
2.1 铝合金碱蚀反应机理
铝在碱蚀槽液中发生的反应为:
去除自然氧化膜的反应 Al
2O
3+2NaOH= 2NaAlO
2+H
2O (l)
;铝基体的反应 2Al+2NaOH+ 2H
2O= 2NaAlO
2+3H
2↑ (2)
上面的(l)
和(2)
反应都有NaAlO
2生成。当溶液中铝离子过多时,会致使NaAlO
2,水解生成Al
(OH)
3沉淀。在碱蚀槽液中由于有大量苛性钠的存在,铝会变成铝离子,其主要是以AlO
2-的形式存在于溶液中。但当pH
为8.0
~10
时,根据c(Al
3+)= K
sp/c
(OH
-)3=1.3×10
-33/c
(OH
-)3计算可知,铝离子几乎全部以Al(OH)
3的形式存在;而当pH
值为3.5
时,溶液中铝主要又以Al
3+的形式存在。因此,我们可以采用前面提到的3
种方法进行测定。
2.2 实验试剂
铝标准溶液:1. 000 g
含99. 8%
以上的纯铝,用35mL25% NaOH
溶液溶解,用蒸馏水定容至250.0mL
,摇匀,配成4 mg/mL
的溶液;
盐酸标准溶液:两份,浓度c( HCl)
分别为l.5 mol/L
、0.1 mol/L
;
NaOH
标准溶液:浓度c(NaOH)
为0.6 mol/L
;
EDTA
标准溶液:浓度c(EDTA)
为0.1 mol/L
;
锌盐标准溶液:分析纯的锌用盐酸溶解,浓度c
(Zn
2+)为0.1 mol/L
;
酒石酸钾钠溶液:浓度为2%
;
氟化钾溶液:浓度为2%
;
酚酞溶液:浓度为0.2%
;
甲基橙溶液:浓度为0.2%
;
二甲酚橙溶液:浓度为0.2%
;
六次甲基四胺缓冲溶液:将pH
值为5.4
的试剂400 g
溶于蒸馏水中,加入1 mol/L
的盐酸100 mL
,定容到1L
,摇匀。
采用不同方法测定时,所用的标准溶液的浓度均不同,可根据各种方法所消耗的量来调节标准溶液的浓度。若其浓度为x%
时,则表示100 mL
溶液中溶解了x g
的溶质。
2.3 单指示剂方法
在酒石酸钾钠过量存在下,用盐酸滴定总碱,然后加入氟化钾,氢氧化铝与氟离子结合放出氢氧根离子,再用盐酸滴定这些氢氧根离子,可计算出铝离子的量。具体反应为:
NaOH+ HCl→NaCl+ H
2O
Al(OH)
4-+H
++4(C
4H
4O
6)
42-→[Al(OH)
3(C
4H
4O
6)
4]
8-+H
2O
[Al(OH)
3(C
4H
4O
6)
4]
8-+6F
-→AlF
63-+3OH
-+4(C
4H
4O
6)
42-
3OH
-+3H
+→3H
2O
实验步骤为:用移液管准确吸取碱蚀液5.00 mL
于250 mL
锥形瓶中,加入30 mL
酒石酸钾钠溶液和50 mL
蒸馏水,再加入2
滴酚酞指示剂,然后用盐酸标准溶液(c(HCl)
为1.5 mol/L
)滴定至红色消失为终点,记下滴定读数为V
1,最后加入20 mL
氟化钾溶液(此时溶液再显红色),继续用盐酸标准溶液(浓度同上)滴定至红色消失为终点,记下滴定读数为V
2。计算式为:
铝c(Al)=27c(HCI) V
2/( 3×5.00)( g/L)
游离碱 c
(NaOH
)=40c(HCl)( V
1-V
2)/5.00(g/L)
2.4 双指示剂方法
从铝合金碱蚀反应机理可知,当pH
值为3.5-9
时,碱蚀中铝的定量反应为:Al
3++3OH
-=Al(OH)
3↓
,可用酚酞和甲基橙双指示剂来指示其滴定终点,而它们变色的pH
值范围分别为8.0~9.6
和3.1~4.4
。当溶液以酚酞为指示剂,用盐酸标准溶液滴定至溶液为无色时,溶液pH
值为9.0
,其发生的反应为:
NaOH+HCl→NaCl+H
2O
Al(OH)
4-+H
+→Al(OH)
3↓+H
2O
此时溶液中游离碱的量可由消耗的盐酸量来求得。
当溶液以甲基橙为指示剂,用盐酸标准溶液滴定至溶液为红色变黄色时,溶液的pH
值即为3.5
,溶液除了发生上述反应外,还发生如下反应:Al(OH)
3+3H
+→Al
3++3H
2O
此时溶液中消耗的盐酸量即为游离碱的量和铝离子的量之和,由此可计算出铝离子的含量。
由此可见,用酚酞和甲基橙双指示剂,以HCl
溶液为标准溶液测定碱蚀液中游离碱的量和铝离子的含量是可靠的。但为了提高测定的准确性和便于观察,我们可在溶液中先加入过量的盐酸标准溶液,然后以NaOH
溶液为标准溶液来返滴定。为了避免pH
值为3.5
时Al
3+以Al(OH)
3形式析出,100 mL
被测定的溶液中铝含量以不大于100 mg
为宜。
实验步骤为:用移液管准确吸取碱蚀液2.00 mL
,2
份,分别放于两只250 mL
锥形瓶中,加入100 mL
蒸馏水,再准确加入盐酸标准溶液( c(HCl)
为l.5 mol/L
)20.00 mL
摇动至溶液澄清。其中一份溶液加入2
滴酚酞指示剂,用NaOH
标准溶液滴定至淡红色即为终点,记下滴定读数为V
1;另一份溶液加入2
滴甲基橙指示剂,用NaOH
标准溶液滴定至溶液由红色变黄色为终点,记下滴定读数为V
2。计算式为:
铝 c(Al)=27 c(NaOH)(V
1-V
2)/(32.00) (g/L)
游离碱 c(NaOH)=40[c (HCl)15.00-c(NaOH)V
1]/2.00(g/L)
2.5 DTA络合滴定法
滴定时,若以酚酞为指示剂,用盐酸标准溶液滴定至溶液为无色时,溶液的pH
值即为9.0
。根据上述原理可知,此时溶液中消耗盐酸的量即为游离碱的量,据此可计算出游离碱的含量。然后加入缓冲溶液,用EDTA
进行络合滴定,消耗EDTA
的量即为铝离子的量。为了测定的准确与方便,本文采用先加入过量的EDIA
,然后再用锌标准溶液滴定过量的EDTA
。从而可计算出铝离子的含量。
实验步骤为:用移液管准确吸取碱蚀液10.00 mL
于100 mL
的容量瓶中,定容至100.0 mL
,从容量瓶中准确移取10. 00 mL
于250 mL
锥形瓶中,再加入100 mL
蒸馏水,然后加入2
滴酚酞指示剂,用盐酸标准溶液(c( HCl)
为0.1 mol/L
)滴定至红色消失为终点,记下滴定读数为V
1;然后加入六次甲基四胺缓冲液25 mL
,摇匀,再加入EDIA
标准溶液50.00 mL
,加热煮沸2
分钟,冷却,再加入二甲酚橙指示剂1
滴,最后用锌标准溶液滴定至黄色变玫瑰红为终点,记下所消耗的锌标准溶液的体积V
。计算式为:
铝含量 c(Al)=27[c(EDIA)50.00-c(Zn
2+) V
2]/1.00(g/L
)
游离碱 c(NaOH)= 40c(HCl)V
1/1.00( g/L)
2.6 回收试验
在上述的测定方法中,加入10.00 mL
铝标准溶液,测定铝的回收率。而加入5.00 mL
相应的NaOH
标准溶液测定游离碱的回收率。
3 实验结果与讨论
采用上述三种不同的滴定分析方法分别对同一碱蚀液中游离碱浓度和铝含量进行测定,每种方法都平行测定6
次,并对6
次测定的数据进行了误差分析,分别计算了其平均值、标准偏差和变异系数,最后以平均值和标准偏差来表示分析的结果,其有关数据见表1。
表1 碱蚀液中铝离子和游离碱的含量及回收率
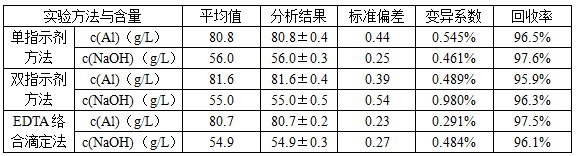
从表1数据来看,EDTA络合滴定法和双指示剂方法测定的游离碱含量较接近,分别为54.9 g/L和55.0 g/L。从误差分析来看,EDTA络合滴定法的精密度比双指示剂方法高,而回收率则差别不大。单指示剂方法测出的游离碱的含量为56.0 g/L,与其它两种方法测出的结果相差较大,但误差分析的结果表明,其精密度均高于其它两种方法,且回收率也高一点。
从碱蚀液中铝含量的测定结果来看,单指示剂方法和EDTA络合滴定法测定结果较接近,分别为80.8g/L和80.7g/L。误差分析的结果表明,EDTA络合滴定法的精密度比单指示剂方法好,回收率也较高。双指示剂方法测得的结果与前两种方法所得的结果相差则较大,结果为81.6 g/L,精密度则比单指示剂方法好而比EDTA络合滴定法差,回收率比两者都要低。
从上述分析可知,测定碱蚀液中游离碱的含量时,单指示剂方法最好,EDTA络合滴定法次之,双指示剂方法则最差。这可能是因为选用双指示剂来区分pH值在3.5~9之间的界限,滴定时对终点的观察和判断较为模糊,致使双指示剂方法测定的精密度低一些。单指示剂方法从其测定的原理来看较为合理。测定时的终点也较明显清晰,但测定铝含量时终点不好观察,这可能是使其测定铝含量的结果误差较大的主要原因。
从以上分析还可知,测定碱蚀液中铝含量时,双指示剂方法最差,EDTA络合滴定法最好。单指示剂方法和双指示剂方法都是利用铝离子具有酸碱两性的性质进行设计的方法,采用的都是酸碱滴定法的原理,所以结果准确性会差一些,而EDTA络合滴定法是应用EDTA的络合原理只针对铝离子进行测定,实验结果的精密度和准确性都较好,但由于不同的厂家所用的碱蚀添加剂的组成不同,如果添加剂中含有络合铝离子的能力强于EDTA,可能会使测定的结果偏低,实验结果的准确性也降低。
从三种方法的操作步骤和所用的试剂来看,单指示剂方法的操作步骤最简便,只用酸式滴定管就可完成,终点的观察也不难,只用到盐酸、酒石酸钾钠、氟化钾、酚酞等试剂,因此所用的试剂也不多。双指示剂方法由于要同时测定两份溶液,且要使用两种指示剂,操作上稍为复杂一点,但步骤也较简单,只用碱式滴定管即可完成,而且只用到盐酸、氢氧化钠、酚酞和甲基橙等试剂,测定成本相对前者要便宜一些。EDTA络合滴定法相对前两种方法,操作步骤最复杂,所用到的试剂也比较多,对工厂的操作人员要求也会高一些。
综上所述,从分析结果的准确性来看,三种方法均能满足生产上所需要的要求。但从分析测定的快速、简便性以及成本来考虑,测定碱蚀槽液中游离碱的浓度和溶解铝含量最好的方法还是单指示剂方法,其次是双指示剂方法,而对一些要求较高的厂家则可采用EDTA络合滴定法。
4 结论
采用单指示剂方法、双指示剂方法和EDTA络合滴定法这三种方法对碱蚀槽液中游离碱的浓度和溶解铝含量进行测定的结果表明:测定碱蚀液中游离碱的含量时,单指示剂方法最好,EDTA络合滴定法次之,双指示剂方法则最差;测定碱蚀液中铝含量时,双指示剂方法最差,单指示剂方法次之,EDTA络合滴定法最好;三种方法测定结果的准确性和精密度均能满足铝合金氧化加工生产的要求:从操作步骤和所用的试剂来分析,单指示剂方法的操作步骤最简单,而EDTA络合滴定法的操作步骤最复杂,所用到的试剂也比较多。由此可见,铝阳极氧化碱蚀槽液中游离碱浓度和铝含量的测定最好的方法是单指示剂方法,其次是双指示剂方法,再次是EDTA络合滴定法。
